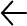Importancia de la rifaximina en pacientes con sindrome de intestino irritable
El síndrome del intestino irritable (SII) es un trastorno gastrointestinal funcional crónico caracterizado por dolor abdominal recurrente y patrones intestinales anormales. La alteración de la flora intestinal, la hipersensibilidad visceral y la motilidad intestinal anormal hacen parte de la compleja fisiopatología del SII.
La rifaximina es un antimicrobiano no absorbible de amplio espectro que inhibe la síntesis de ARN bacteriano al unirse a la subunidad ß de la ARN polimerasa microbiana. Se dirige al tracto gastrointestinal y actúa reduciendo la cantidad de bacterias productoras de gas y alterando las especies predominantes de bacterias presentes.
PORCENTAJE DE PACIENTES CON ALIVIO DE LOS SÍNTOMAS DURANTE EL PERIODO DE EVALUACIÓN TEMPRANA (3–6 semanas)

Se ha demostrado que la rifaximina mejora los síntomas generales del SII, como hinchazón, flatulencia, dolor abdominal y consistencia de las heces. Como fármaco antimicrobiano no absorbible, se dirige al tracto gastrointestinal con efectos sistémicos mínimos. El Colegio Americano de Gastroenterología emitió una declaración basada en evidencia de que la rifaximina es eficaz para reducir los síntomas totales del SII, así como la hinchazón en el SII-D.
Referencias
1.Profile of rifaximin and its potential in the treatment of irritable bowel syndrome. Natalya Iorio, Zubair Malik, and Ron Schey. Clin ExpGastroenterol. 2015; 8: 159–167. Disponible en: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4467648/
IBS KOL-LEAGUE PROF. Dr. Serhat Bor – Bodep part 1
Resolviendo desafíos en el diagnostico IPE
Speaker: Dr.Enrique Dominguez
Fecha: 10 de abril
La importancia de la salud gastrointestinal de los deportistas
Los deportistas requieren de un intestino que funcione adecuadamente, puesto que, le ayudará a tener un buen desempeño en los entrenamientos, permitiéndole así, llevar a cabo competencias con éxito, sin tener que llegar a abandonarlas por nauseas, cólicos intestinales o alteración en sus evacuaciones1.
Una de las principales causas de abandono de competencias son los malestares gastrointestinales como nauseas y/o vomito, y aunque se han identificado algunos suplementos dietarios que proveen múltiples beneficios para los atletas, otros, pueden llevar a eventos adversos gastrointestinales, que impactan en los entrenamientos y el rendimiento1.
El principal interés de los probióticos en los atletas consiste en generar un ambiente intestinal adecuado, que permita reducir los síntomas gastrointestinales durante la competencia y los entrenamientos, y prevenir o reducir los días de enfermedades infecciosas. Los mecanismos por los que los probióticos pueden contribuir a esos intereses son a través de la modulación del sistema inmunológico, la gran capacidad de adhesión a la mucosa, la estabilización de la función de la barrera gastrointestinal, la mejoría en la absorción de nutrientes, y la producción de ácidos grasos de cadena corta 1,2,3.
Ahora bien, a la hora de elegir un probiótico para un deportista hay que tener en cuenta 3 puntos, en primer lugar, respecto a la eficacia, las cepas más estudiadas son las de género Bifidobacterium y Lactobacillus, por lo que son las más fiables para este caso en específico teniendo en cuenta la evidencia científica, en segundo lugar, respecto a seguridad, los probióticos se consideran seguros en personas sanas, y en tercer lugar, se ha considerado que para recibir los beneficios de los probióticos, es importante una duración mínima de uso de 2 a 4 semanas 1,2.
Teniendo en cuenta lo anterior, las cepas probióticas Lacticaseibacillus rhamnosus GG (LGG) y Bifidobacterium animalis subp. Lactis (BB-12) de los géneros previamente mencionados, han demostrado ser eficaces en la disbiosis; a través de un efecto sinérgico en la adhesión a la mucosa gastrointestinal, normalizando la permeabilidad gastrointestinal, inhibiendo la adhesión de patógenos, produciendo péptidos antibacterianos, además de que han evidenciado reducir los días de diarrea en hasta un 2.2 días, lo que los hace una buena alternativa, a la hora de permitir al deportista entrenar sin interrupciones, y mantener una flora gastrointestinal adecuada que contribuya a su buen desempeño2,3,4.
Para más información sobre suplementos en deportistas ingrese al siguiente link:
https://pubmed.ncbi.nlm.nih.gov/34814219/
Referencias
- Wilson P. Sport Supplements and the Athlete’s Gut: A Review. Int J Sports Med. 2022;43(10):840-849. doi:10.1055/a-1704-3086
- Guarner, F., Sanders, M. E., & Szajewska, H. (2023). Probiotics and prebiotics; World Gastroenterology Organisation Global Guidelines. https://www.worldgastroenterology.org/guidelines/probiotics-and-prebiotics/probiotics-and-prebiotics-english
- Grenov B, Namusoke H, Lanyero B, et al. Effect of Probiotics on Diarrhea in Children With Severe Acute Malnutrition: A Randomized Controlled Study in Uganda. J Pediatr Gastroenterol Nutr. 2017;64(3):396-403. doi:10.1097/MPG.0000000000001515
- Collado MC, Meriluoto J, Salminen S. Role of commercial probiotic strains against human pathogen adhesion to intestinal mucus. Lett Appl Microbiol. 2007;45(4):454-460. doi:10.1111/j.1472-765X.2007.02212.x
Insuficiencia pancréatica exocrina
Mecanismo de acción
Resolviendo desafíos en el diagnóstico de la insuficiencia pancreática exocrina
Conferencia virtual en vivo realizada el Miércoles 10 de Abril, dictada por el Doctor Enrique Dominguez reconocido gastroenterólogo y que hizo parte del equipo que desarrolló, validó, publicó e implementó esta importante herramienta. Quien nos compartió en esta conferencia su experiencia en el desarrollo de esta iniciativa.
Potente sinergia de LGG® + BB12® como probioticoterapia
Probióticos: vitales en la protección gastrointestinal
Los probióticos poseen varios efectos beneficiosos demostrados sobre la salud humana a lo largo de toda la vida desde el nacimiento. Estos efectos incluyen: mantener el desarrollo saludable de la microbiota intestinal, corregir las alteraciones observadas en las enfermedades inflamatorias intestinales y contrarrestar los cambios en la microbiota que preceden a estos trastornos.1,2
La mayoría de estudios y aplicaciones clínicas de los probióticos se han relacionado con el manejo de infecciones gastrointestinales (GI) causadas por microorganismos patógenos sobre anomalías inflamatorias de la microbiota. 3

Combinación sinérgica de LGG®+BB12®
Las combinaciones de probióticos pueden tener efectos aditivos y sinérgicos; dos cepas particulares en combinación, Lactobacillus rhamnosus GG (LGG®) y Bifidobacterium lactis (BB12®), han sido evaluadas como efectivas en diferentes tipos de gastroenteritis. Más aún,la presencia de LGG® mejora significativamente la adhesión de BB12®, y esta combinación ha demostrado incluso eficacia en el manejo de condiciones como la enfermedad diarreica aguda (EDA).2
Estudios preclínicos han demostrado que tanto LGG® como BB12® se unen de manera importante a la mucosa de todo el tracto GI analizado (desde el duodeno hasta el colon descendente); en general, la presencia de la otra cepa probiótica incrementó los porcentajes de adhesión de ambas cepas, principalmente en intestino grueso (ver Figura). Asimismo, la combinación sinérgica redujo la adhesión patógena en todas las mucosas analizadas en el estudio (especies inhibidas: E. coli, C. difficile y S. enterica).4
Algunos estudios destacados de la combinación LGG®+BB12® han mostrado además que:
LGG® posee una alta adherencia a la mucosa gastrointestinal, propiedad vital que contribuye a inhibir, desplazar y competir con la adhesión de patógenos a la mucosa.3
LGG® aumentó significativamente la respuesta inmune humoral a la enteritis por rotavirus; además, la adhesión de BB12® mejoró en presencia de LGG® en niños sanos y durante episodios de diarrea, lo que reafirma que la acción de los dos probióticos resulta ser sinérgica.1
Un estudio que evaluó el uso de LGG®+BB12® en niños con desnutrición aguda severa y disbiosis de la microbiota, demostró que la combinación sinérgica aumentó el número de especies de probióticos observadas en heces posterior al tratamiento, y redujo sustancialmente la incidencia acumulada de diarrea durante el periodo de seguimiento.5
Referencias
1. Cruchet S, Furnes R, Maruy A, et al. The Use of Probiotics in Pediatric Gastroenterology: A Review of the Literature and Recommendations by Latin-American Experts. Pediatr Drugs. 201 Salminen S, Dvm YB, de Vos W. Intestinal colonisation, microbiota and future probiotics? Asia Pac J Clin Nutr. 2006;15(4):558-56
2. Salminen S, Dvm YB, de Vos W. Intestinal colonisation, microbiota and future probiotics? Asia Pac J Clin Nutr. 2006;15(4):558-562.
3. Collado MC, Jalonen L, Meriluoto J, Salminen S. Protection mechanism of probiotic combination against human pathogens: in vitro adhesion to human intestinal mucus. Asia Pac J Clin Nutr. 2006;15(4):570-575.
4. Collado MC, Grzeskowiak Ł, Salminen S. Probiotic Strains and Their Combination Inhibit In Vitro Adhesion of Pathogens to Pig Intestinal Mucosa. Curr Microbiol. 2007;55(3):260-265. doi:10.1007/s00284-007-0144-8
5. Castro-Mejía JL, O’Ferrall S, Krych Ł, et al. Restitution of gut microbiota in Ugandan children administered with probiotics ( Lactobacillus rhamnosus GG and Bifidobacterium animalis subsp. lactis BB-12) during treatment for severe acute malnutrition. Gut Microbes. 2020;11(4):855-867. doi:10.1080/19490976.2020.1712982
Sinergia probiótica superior con respaldo científico
Recomendaciones del Grupo de Interés Especial en Microbiota Intestinal de la European Society for Paediatric Gastroenterology, Hepatology and Nutrition (ESPGHAN) de 2023, sobre el uso de probióticos para el manejo de trastornos gastrointestinales (TGI) pediátricos.
De acuerdo con las nuevas recomendaciones de la ESPGHAN, sobre el uso de probióticos en el tratamiento de TGI pediátricos, se han resaltado directrices específicas referentes a BB-12® bifidobacterium animalis subsp. lactis / LGG® Lactobacillus rhamnosus en comparación con Bacillus clausii (B. clausii):1

- Varios estudios han demostrado la eficacia de LGG® para reducir la duración de la diarrea viral aguda y la diarrea infecciosa aguda.2
- Se ha demostrado que LGG® disminuye la duración de la hospitalización, tanto en niños eutróficos como con desnutrición severa.2
- LGG® también se ha asociado con una reducción significativa en la excreción de rotavirus.2
Referencias
1. Szajewska H, Berni Canani R, Domellöf M, et al. Probiotics for the Management of Pediatric Gastrointestinal Disorders: Position Paper of the ESPGHAN Special Interest Group on Gut Microbiota and Modifications. J Pediatr Gastroenterol Nutr. 2023;76(2):232-247. doi:10.1097/MPG.0000000000003633
2. Cruchet S, Furnes R, Maruy A, et al. The Use of Probiotics in Pediatric Gastroenterology: A Review of the Literature and Recommendations by Latin-American Experts. Pediatr Drugs. 2015;17(3):199-216. doi:10.1007/s40272-015-0124-6
LGG® Y BB12®, Una eficaz combinación probiótica contra la diarrea aguda en todos los grupos etarios
Numerosos estudios llevados a cabo en distintas ciudades del mundo han validado la eficacia terapéutica, tanto en población pediátrica como adulta, de los probióticos Lactobacillus rhamnosus GG (LGG®) y Bifidobacterium animalis subsp. Lactis (BB12®) para el tratamiento y prevención de enfermedades gastrointestinales. De hecho, existen más de 1.100 publicaciones que respaldan el uso terapeútico del LGG® y más de 300 que avalan al BB12®, de las cuales 300 y 180 publicaciones, respectivamente, son estudios clínicos.1,2 Gracias a esto, múltiples organizaciones y asociaciones de expertos y especialistas han plasmado en documentos oficiales, guías de práctica clínica y pautas institucionales, la recomendación de implementar estas cepas para la prevención y el tratamiento de distintas afecciones agudas del sistema digestivo.3-6
En cuanto a la enfermedad diarreica aguda (EDA), su alta incidencia en todos los grupos etarios puede perjudicar la calidad de vida y bienestar del paciente si no es tratada de manera adecuada,7 por lo cual un tratamiento probiótico de esta índole puede presentar beneficios4-6 como la disminución de los días con deposiciones diarreicas y el apoyo a la estabilización de la hidratación y la microbiota intestinal. A continuación, se explicará con mayor detalle los beneficios que presenta esta combinación.
La complementación entre LGG® Y BB12®
No es producto del azar que estas cepas funcionen excepcionalmente al combinarse, ya que los méritos individuales de cada una para los tratamientos gastrointestinales son contundentes en este campo: el LGG® es el probiótico más estudiado en el tratamiento de EDA a nivel mundial, además de ser la cepa que mayor adhesión y resistencia ha demostrado en el tracto gastrointestinal,1 mientras que el BB12® es la bifidobacteria más estudiada para el fortalecimiento del sistema inmune.2,8,9
La naturaleza de la sinergia en esta combinación se basa en el incremento en la adherencia a la mucosa intestinal de cada cepa,10-12 induciendo un mayor desplazamiento de patógenos debido a esa mayor adherencia competitiva.1,2,10,11,13-18 Desde el año 2000 existe evidencia de que la combinación de las dos cepas permite una mayor adhesión a la mucosa intestinal que por separado19 y en el 2007, Collado et al. demostraron mediante un modelo animal in vitro que esta combinación lograba una mayor adhesión en el colon que las presentaciones individuales de LGG® y BB12® (gráficas 1 y 2).20 Además de eso, ambas fortalecen la función de la barrera intestinal a través de mecanismos complementarios: el LGG® a través de la producción de proteínas,21 y el BB12® a través del fortalecimiento de las uniones estrechas.22

Uso de la combinación de LGG® Y BB12® en caso Enfermedad diarreica Aguda.
Si bien cada cepa se ha estudiado robustamente de manera individual, su combinación también está respaldada por evidencia clínica. Por ejemplo, en el 2017 Grenov et al. realizaron un estudio aleatorizado, doble ciego, controlado con placebo, el cual incluyó a 400 niños hospitalizados con desnutrición aguda severa (DAS) en el país africano de Uganda, que padecían diarrea aguda junto a otras complicaciones sintomáticas. Los pacientes fueron distribuidos en dos grupos que recibieron el tratamiento estándar de suero de rehidratación oral (SRO) junto a una (1) dosis diaria de la mezcla de LGG® y BB12® (1×1010 millones de unidades formadoras de colonias, 50:50) o de placebo durante la hospitalización, seguido de un período de tratamiento ambulatorio de 8 a 12 semanas. El desenlace primario fue el número de días con diarrea durante la hospitalización, mientras que entre los objetivos secundarios se tuvo la disminución de días con diarrea a nivel de consulta externa.23
Como puede observarse en la gráfica 3, durante el tratamiento ambulatorio de consulta externa la combinación probiótica logró una reducción adicional de 2,2 días en la duración promedio del episodio diarreico (intervalo de confianza del 95%; diferencia ajustada: 3,5 a 0,3; p = 0,025). Es decir, la combinación de LGG® y BB12® redujo el número de días con diarrea en un 26%, lo cual indica que esta combinación puede tener un papel importante en el tratamiento de los niños hospitalizados con diarrea y desnutrición severa.23 Gracias a esto, podría contemplarse una hipótesis que requeriría confirmación bajo estudios comparativos en poblaciones de características homogéneas, sobre si la magnitud de este resultado podría deberse a la acción sinérgica de la combinación LGG® + BB12®; considerando que según el metanálisis de Szajewska et al.24 del 2013, LGG® por sí solo puede reducir la duración de la diarrea en 1,05 días (intervalo de confianza del 95%; diferencia ajustada: 1,7 a 0,4), mientras que en el estudio bajo discusión la reducción lograda por la combinación LGG® + BB12® fue de 2,2 días.23

De esta manera, el estudio de Grenov B, et al. se convirtió en un precedente relevante, que cimienta las bases para futuros ejercicios de comparabilidad que permitan robustecer aún más los soportes científicos sobre beneficios de esta combinación probiótica.
LGG® Y BB12®, Una eficaz e inigualable combinación probiótica para el tratamiento de la diarrea
A partir de estas consideraciones, se puede evidenciar que para el tratamiento de padecimientos gastrointestinales como la EDA, la combinación de las cepas probióticas LGG® y BB12® cuenta con un amplio dossier que respalda su eficacia terapéutica, debido a que:
Une al probiótico más estudiado en el tratamiento de la EDA y la bifidobacteria más estudiada para el fortalecimiento del sistema inmune.1,2
El uso de la combinación genera un efecto sinérgico en la adhesión a la mucosa gastrointestinal, mejorando el efecto fisiológico de barrera.19,20
Dispone de evidencia clínica de su capacidad, en tratamiento ambulatorio de consulta externa, para lograr una reducción adicional en la duración promedio del episodio diarreico de -2,2 días comparado con placebo.23
Referencias
1. Andersen MB, Gondolg UH. The Science behind Lactobacillus Rhamnosus LGG®. Published by Human Health CHR, Hansen A/S. Denmark.
2. Eskesen D. The Science behind Bifidobacterium BB12®. Published by Human Health CHR, Hansen A/S. Denmark.
3. Guarino A, et al. European Society for Pediatric Gastroenterology, Hepatology, and Nutrition/European Society for Pediatric Infectious Diseases Evidence-Based Guidelines for the Management of Acute Gastroenteritis in Children in Europe: update 2014. JPGN. 2014; 59 (1): 132-152.
4. Cruchet S, Furnes R, Maruy A, Hebel E, Palacios J, Medina F et al. The Use of Probiotics in Pediatric Gastroenterology: A Review of the Literature and Recommendations by Latin-American Experts. Pediatr Drugs. 2015;17:199–216.
5. Guarner F, Sanders ME, Eliakim R, Fedorak R, Gangl A, Garisch J et al. Probióticos y prebióticos. Guía mundial de la Organización Mundial de Gastroenterología. 2017.
6. Salazar Lindo E, Gutiérrez-Castrellón P, Polanco Allué I,Grupo Ibero-Latinoamericano sobre el Manejo de la Diarrea Aguda (GILA). Guía de práctica clínica ibero-latinoamericana sobre el manejo de la gastroenteritis aguda en menores de 5 años: enfoque, alcances y diseño. An Pediatr (Barc). 2014;80 (Supl 1): 9-14.
7. Román Riechmann E, et al. Diarrea aguda. Protocolos diagnóstico-terapéuticos de Gastroenterología, Hepatología y Nutrición Pediátrica SEGHNPAEP. Disponible en: https://www.aeped.es/sites/default/files/documentos/diarrea_ag.pdf
8. Vernazza CL, Gibson GR, Rastall RA. Carbohydrate preference, acid tolerance and bile tolerance in five strains of Bifidobacterium. J.Appl.Microbiol. 2006;100:846-853.
9. Laparra JM,Sanz Y. Comparison of in vitro models to study bacterial adhesion to the intestinal epithelium. Lett.Appl.Microbiol. 2009;49:695-701.
10. Biller JA, Katz AJ, Flores AF, Buie TM, Gorbach SL. Treatment of recurrent Clostridium diffcile colitis with Lactobacillus GG. J Pediatr Gastroenterol Nutr. 1995 Aug;21(2):224-6.
11. Segers ME, Sarah Lebeer S. Towards a better understanding of Lactobacillus rhamnosus GG – host interactions. Microbial Cell Factories 2014, 13(Suppl 1):S7.
12. Grönlund MM, Gueimonde M, Laitinen K, Kociubinski G, Grönroos T, Salminen S et al. Maternal breast-milk and intestinal bifdobacteria guide the compositional development of the Bifdobacterium microbiota in infants at risk of allergic disease. Clin Exp Allergy. 2007 Dec;37(12):1764-72.
13. Ganguli K, et al. Lactobacillus rhamnosus GG and its SpaC pilus adhesin modulate inflammatory responsiveness and TLR-related gene expression in the fetal human gut. Pediatr Res. 2015 April ; 77(4): 528–535.
14. Kankaanpää P, Sütas Y, Salminen S, Isolauri E, Arvilommi H. Results on Clinical Demonstrations of Probiotics on Children. Functional Food Research in Europe: 3rd Workshop, Technical Research Centre of Finland, 1998.
15. De Vrese M, Rautenberg P, Laue C, Koopmans M, Herremans T, Schrezenmeir J. Probiotic bacteria stimulate virusspecifc neutralizing antibodies following a booster polio vaccination. Eur J Nutr. 2005 Oct;44(7):406-13.
16. Sindhu KN, Sowmyanarayanan TV, Paul A, Babji S, Ajjampur SS, Priyadarshini S et al. Immune response and intestinal permeability in children with acute gastroenteritis treated with Lactobacillus rhamnosus GG: a randomized, double-blind, placebo-controlled trial. Clin Infect Dis. 2014 Apr;58(8):1107-15.
17. Kaila M, Isolauri E, Saxelin M, Arvilommi H, Vesikari T. Viable versus inactivated lactobacillus strain GG in acute rotavirus diarrhoea. Arch Dis Child. 1995 Jan;72(1):51-3.
18. Myllyluoma E, Kajander K, Mikkola H, Kyrönpalo S, Rasmussen M, Kankuri E et al. Probiotic intervention decreases serum gastrin-17 in Helicobacter pylori infection. Dig Liver Dis. 2007 Jun;39(6):516-23.
19. Ouwehand AC, Isolauri E, Kirjavainen PV, Tolkko S, Salminen SJ. The mucus binding of Bifidobacterium lactis Bb12 is enhanced in the presence of Lactobacillus GG and Lact. delbrueckii subsp. Bulgaricus. Letters in Applied Microbiology. 2000; 30: 10–13
20. Collado MC, Meriluoto J, Salminen S. Role of commercial probiotic strains against human path-ogen adhesion to intestinal mucus. Lett.Appl.Microbiol. 2007a;45:454- 460.
21. Lu R, Fasano S, Madayiputhiya N et al. Isolation, identification, and characterization of small bioactive peptides from Lactobacillus GG conditional media that exert both anti-Gram-negative and Gram-positive bactericidal activity. J Pediatr Gastroenterol Nutr 2009; 49(1):23-30
22. Commane DM, Shortt CT, Silvi S, Cresci A, Hughes RM, Rowland IR. Effects of fermentation products of pro- and prebiotics on trans-epithelial electri-cal resistance in an in vitro model of the colon. Nutr.Cancer 2005;51:102-109.
23. Grenov B, et al. Effect of probiotics on diarrhea in children with severe acute malnutrition: a randomized controlled study in Uganda. J Pediatr Gastroenterol Nutr. 2017;64(3):396-403.
24. Szajewska H, et al. Meta-analysis: Lactobacillus GG for treating acute gastroenteritis in children – updated analysis of randomised controlled trials. Aliment Pharmacol Ther. 2013;38(5):467-76.